高中化学原电池是什么(化学能转电能,原电池效率揭秘!)
电化学中的原电池和能量转化
导言: 亲爱的同学们,大家好!我是你们的化学小李老师。在今天的课程中,我们将开始学习电化学的内容。首先,让我们来看一下原电池的部分。通过一个示意图,我们将深入探讨其中的自发氧化还原反应及能量转化。
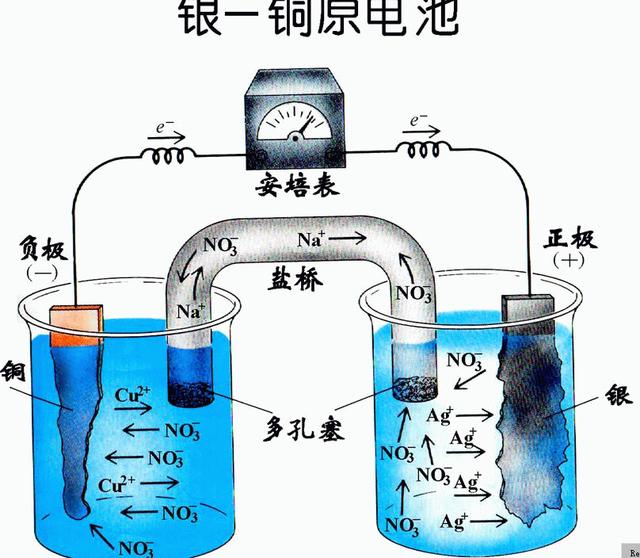
自发氧化还原反应的观察
在这个示意图中,大家是否能找到一个自发的氧化还原反应?是的,我们可以发现锌和两个氢离子之间发生了自发的氧化还原反应。具体来说,锌和两个氢离子反应,生成锌离子和氢气。根据这个反应,我们可以推断锌从零价变成正二价需要失去两个电子,而两个氢离子变成氢气则需要获得两个电子。因此,锌失去的两个电子正好转移给了氢离子,使得氧化还原反应自发进行。
电子转移的方向性比喻
接下来,让我们通过一个简单易懂的比喻来理解电子转移的方向性。想象一下高峰时段大家都急于上公交车,如果大家挤破了头都往车门涌,上车会更快,还是有序地一个一个上车会更快呢?显然,有序地一个一个上车会更加迅速。类比到电子转移上,如果电子都堵在锌的表面,就像大家都挤在车门口,氢离子获取电子的速度会变慢。而如果电子通过导线有序地从锌到达碳的一侧,就如同乘客有序地上车,那么氢离子获取电子的速度就会更快。因此,在这个装置中,虽然氢离子在锌的一侧也能获得电子,但绝大多数情况下,电子会从碳的一侧转移给氢离子。
定向移动的电子和电流形成
通过导线传递的电子形成了定向移动,从而产生了电流。如果我们在导线上接上一个小灯泡,由于电流的形成,小灯泡将会亮起。这样的化学能转化为电能的装置就是原电池。
太阳能电池与原电池的区别
请注意,太阳能电池不是原电池。原电池是将化学能转化为电能,而太阳能电池是将太阳能转化为电能。因此,这两者有本质的区别。
能量转换的限制
然而,需要注意的是,原电池中的能量转化并非百分之百有效。当电池使用时间较长时,你可能会觉得电池变得有些热。这是因为一部分能量以热的形式释放出来,而无法完全转化为电能。
结语: 总之,化学能转化成电能的装置被称为原电池。通过自发的氧化还原反应和定向移动的电子,我们可以在电路中形成电流,将化学能转化为电能。但要记住,能量转化总是受到一定的限制。
致谢: 感谢大家的聆听,我会每天与大家分享更多有关化学的知识。如果你理解了以上内容,请双击以示加哦。
